我院闫道广/钟文彬课题组对肿瘤发生机制的突破性研究在顶级期刊Science Translational Medicine和Blood上连续发表
2022-02
文章来自:生命科学技术学院 阅读次数:1394
近日,我校生命科学技术学院闫道广/钟文彬课题组在肿瘤发生机制的突破性研究成果"Loss of miR-31-5p drives hematopoietic stem cell deterioration and restoration eliminates leukemia stem cells"和"Oxysterol-binding protein-related protein 4L (ORP4L) is a prerequisite for the induction of T-cell leukemogenesis associated with human T-cell leukemia virus 1 (HTLV-1)"分别被Science专业子刊Science Translational Medicine和血液学顶级期刊Blood发表。暨南大学为这两篇论文的唯一第一作者和通讯作者单位。

论文在Science Translational Medicine杂志发表

论文在Blood杂志发表
白血病(Leukemia)在儿科恶性肿瘤的发病率中居第一位,它的致死率在导致儿童及35岁以下成年人死亡的恶性肿瘤中排首位。揭示它们的发病机制是临床治愈这些疾病的关键。上述两项研究分别从细胞能量代谢重构和磷脂代谢的新视角,阐明了正常造血干细胞和正常T细胞如何恶性转化并形成为髓性白血病和T细胞白血病,研究结果可能为临床带来新的治疗概念和靶点。
Science Translational Medicine发表的文章表明,相比于正常造血干细胞(HSCs),微小RNA miR-31-5p在人类白血病干细胞(LSCs)中表达丢失了。在HSCs中抑制miR-31-5p可促进其靶基因FIH的表达,从而抑制HIF-1α信号通路,导致HSCs的能量代谢模式由糖酵解转化为氧化磷酸化,进而增加了三羧酸循环中间代谢产物延胡索酸的丰度。延胡索酸的增加促进组蛋白的甲基化进而驱使HSCs向LSCs的恶性转化,并在B-NDG重度免疫缺陷小鼠中引发类髓系白血病。随后,研究团队构建了G7聚(胺)纳米级树突状复合体包封的miR-31-5p mimic纳米颗粒,在PDX动物模型中,联合化疗药物Ara-C,该纳米颗粒能有效清除白血病干细胞并治愈部分疾病小鼠,显示出显著的抗白血病效果。籍此,编辑为本研究撰写题为“Targeting transformation”的总结,认为这是治疗人类髓系白血病非常有潜力的新手段。同时,新华社对该研究进行题为“Chinese scientists develop new potential therapy for leukemia”的英文报道。
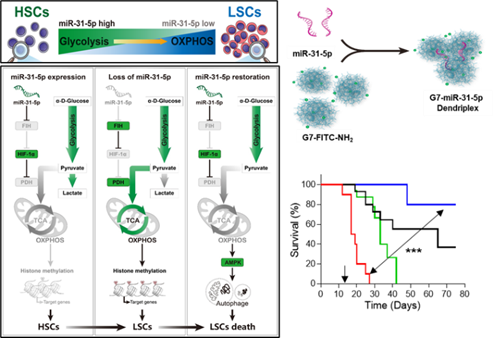
miR-31-5p丢失导致HSC恶性转化,它的再恢复诱导LSCs死亡并治愈小鼠白血病
新华社对该研究进行报道
成人T细胞白血病(ATL)是由1型人类T细胞白血病病毒(HTLV-1)感染引起的侵袭性T细胞恶性肿瘤,患者中位生存期仅为2至6个月,并且目前临床上没有特异针对ATL的治疗药物。Blood的文章揭示一种重要的磷脂酰肌醇(PIPs)转运蛋白ORP4L,在HTLV-1诱导的ATL发生中的关键作用及分子机理。在被HTLV-1感染的CD4+ T细胞中ORP4L被特异诱导表达,其调控细胞膜上PIPs的代谢,促进PI3K/AKT过度激活而诱导T细胞恶性转化。在动物模型中,通过基因编辑手段敲除ORP4L可以完全阻止HTLV-1诱导的T细胞白血病的发生,显示了ORP4L在这个病理过程中不可或缺的关键作用,提供了干预HTLV-1感染人群向T细胞白血病发展和T细胞白血病新的治疗靶点。

ORP4L在HTLV-1诱发的T细胞恶性转化过程中的关键作用
闫道广/钟文彬课题组近年来从脂质信号和能量代谢的角度出发,在肿瘤尤其是病毒相关肿瘤发生和肿瘤细胞生存的机制上做了一系列详细研究:发现了一些有前景的治疗靶点;发表了包括Science Translational Medicine (2022)、 Blood(2021)、Cell Reports (2019)、Nature Communications(2016)、Circulation Research (2016) 等一系列高水平研究论文。
研究工作得到国家自然科学基金、广东省自然科学基金和学校高水平大学建设资金等的支持。
原文链接:
https://www.science.org/doi/10.1126/scitranslmed.abh2548

